
GUÍA PRÁCTICA CLÍNICA:
PARA EL DIAGNÓSTICO Y MANEJO DE LA ANEMIA EN PACIENTES CON ENFERMEDAD RENAL CRÓNICA (2017)
DESCARGAR
VERSIÓN EXTENSA
DESCARGAR
ANEXOS
DESCARGAR
VERSIÓN CORTA
DESCARGAR RECOMENDACIONES Y FLUJOGRAMAS
vacio
vacio
Ámbito
- Esta guía debe ser usada en todos los establecimientos del seguro social del Perú (EsSalud), según lo correspondiente a su nivel de atención.
Población y alcance
- Población: pacientes con enfermedad renal crónica y anemia.
- Alcance: diagnóstico y manejo de anemia en pacientes con enfermedad renal crónica.
Autores
Expertos clínicos:
- Juana Hinostroza Sayas
- Edwin Eduardo Pérez Tejada
- Percy Allan Vidal Orbegozo
- Manuel Llaro Sánchez
- Fernando Mesías Gonzales Haro
- Manuel Ernesto Castillo Zegarra
- Carla Póstigo Oviedo
- Edwin Rolando Castillo Velarde
- Celina Herrera Cunti
- Hugo Gutierrez Casavilca
- Martín Gómez Luján
- Renzo Pavel Valdivia Vega
- Liliana Fernández Anticona
- Bernardo Damaso Mata
- Úrsula Bravo Grados
Metodólogos:
- Lourdes Carrera Acosta
- Rommy Novoa Reyes
Coordinadores:
- Timaná Ruiz, Raúl Alonso
Descargar PDF con más información sobre la filiación y rol de los autores.
Metodología
Resumen de la metodología:
- Conformación del GEG: La Dirección de Guías de Práctica Clínica, Farmacovigilancia y Tecnovigilancia, del Instituto de Evaluación de Tecnologías en Salud e Investigación (IETSI) del Seguro Social del Perú (EsSalud), conformó un grupo elaborador de la guía (GEG), que incluyó médicos especialistas y metodólogos.
- Planteamiento de preguntas clínicas: En concordancia con los objetivos y alcances de esta GPC, se formularon las preguntas clínicas.
- Búsqueda de la evidencia para cada pregunta: Para cada pregunta clínica, se realizaron búsquedas de revisiones sistemáticas (publicadas como artículos científicos o guías de práctica clínica). De no encontrar revisiones de calidad, se buscaron estudios primarios, cuyo riesgo de sesgo fue evaluado usando herramientas estandarizadas.
- Evaluación de la certeza de la evidencia: Para graduar la certeza de la evidencia, se siguió la metodología Grading of Recommendations Assessment, Development, and Evaluation (GRADE), y se usaron tablas de Summary of Findings (SoF).
- Formulación de las recomendaciones: El GEG revisó la evidencia recolectada para cada una de las preguntas clínicas en reuniones periódicas, en las que formuló las recomendaciones usando la metodología GRADE, otorgándole una fuerza a cada una. Para ello, se tuvo en consideración los beneficios y daños de las opciones, valores y preferencias de los pacientes, aceptabilidad, factibilidad, equidad y uso de recursos. Estos criterios fueron presentados y discutidos, tomando una decisión por consenso o mayoría simple. Asimismo, el GEG emitió puntos de buenas prácticas clínicas (BPC) sin una evaluación formal de la evidencia, y mayormente en base a su experiencia clínica.
- Revisión externa: La presente GPC fue revisada en reuniones con profesionales representantes de otras instituciones, tomadores de decisiones, y expertos externos.
Flujogramas que resumen el contenido de la GPC
Flujograma del diagnóstico y manejo

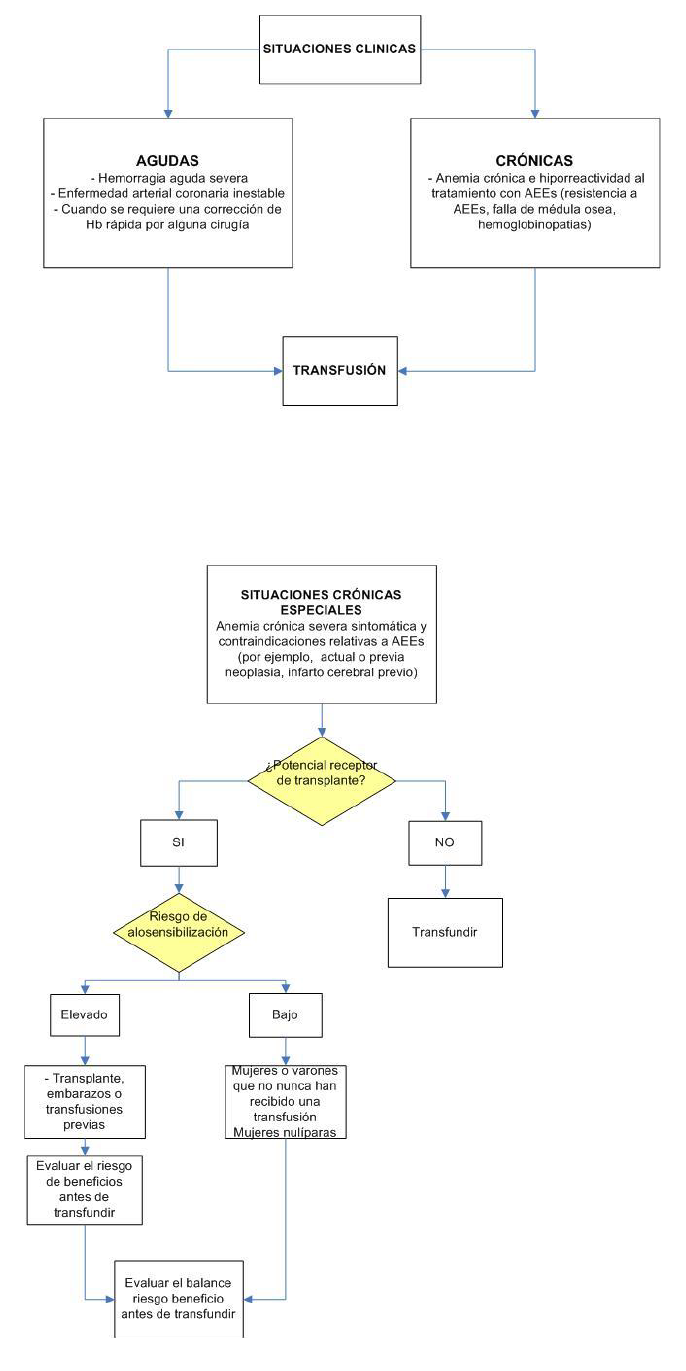
Flujograma de indicación de transfusión en las personas con ERC y anemia
vacio
vacio
1. TFG y anemia
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
En personas con ERC con una TFG menor a 60 mL/min/1.73m2 y anemia, sugerimos investigar la anemia para verificar que sea secundaria a ERC. (Recomendación débil a favor)
BPC 1:
En personas con ERC, el diagnóstico de anemia se define como hemoglobina menor a:
- 12.0 g/dL en mujeres
- 13.0 g/dL en varones
BPC 2:
En pacientes que residen en lugares a más de 1000 metros sobre el nivel del mar, considere la corrección de los valores de hemoglobina para el diagnóstico de anemia, según los valores de OMS.
BPC 3:
Cuando la TFG es mayor o igual a 60 mL/min/1.73m2, pensar que es probable que la anemia se deba a otras causas como deficiencia de ácido fólico o de vitamina B12.
2. Diagnóstico de anemia
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
En personas con ERC y anemia, sugerimos que el diagnóstico de déficit de hierro se realice con alguna de las siguientes pruebas o combinaciones de pruebas:
- La combinación de saturación de transferrina menor del 20% y ferritina sérica menor de 100 microgramos/litro (debiendo cumplir con ambos criterios), o
- El contenido de Hb de reticulocitos (CHr) menor a 29 pg, o
- El porcentaje de glóbulos rojos hipocrómicos (%HRC) mayor al 6%, pero solo si el procesamiento de la muestra de sangre es posible dentro de las 6 horas desde su extracción.
- El contenido de Hb de reticulocitos (CHr) menor a 29 pg , o
(Recomendación débil a favor)
BPC 1:
En personas con ERC, se pueden utilizar las constantes corpusculares (VHCM, CHCM) que se encuentran en el hemograma para evaluar la sospecha de déficit de hierro.
BPC 2:
Realice las pruebas de diagnóstico de déficit de hierro cada 3 meses para personas con ERC que no estén en hemodiálisis crónica, y cada mes para personas con ERC en hemodiálisis crónica.
3. Administración de hierro
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
Para las personas con ERC que no están recibiendo hemodiálisis crónica, recomendamos administrar una prueba de hierro oral antes de ofrecer la terapia de hierro intravenoso. Si el paciente es intolerante al hierro oral o si la Hb objetivo no se alcanza dentro de los 3 meses de terapia con hierro oral, ofrezca terapia de hierro intravenoso. (Recomendación fuerte a favor)
Recomendación 2:
Para las personas que reciben hemodiálisis crónica, recomendamos administrar terapia con hierro intravenoso. La terapia con hierro por vía oral en estas personas puede aplicarse sólo si:
- La terapia con hierro intravenoso está contraindicada o
- La persona decide no recibir tratamiento con hierro intravenoso, después de discutir la eficacia relativa y los efectos secundarios de la terapia con hierro oral e intravenoso.
(Recomendación fuerte a favor)
4. Tratamiento con agentes estimulantes de eritropoyetina
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
En pacientes con ERC y anemia, sugerimos iniciar la administración de AEE si el nivel de hemoglobina (Hb) es menor a 11 g/dL. (Recomendación débil a favor)
BPC 1:
Si existe deficiencia absoluta de hierro, considerar manejar esta deficiencia de hierro antes del inicio de AEE.
BPC 2:
Evaluar de forma individualizada los beneficios y riesgos del uso de AEE, tomando en cuenta las comorbilidades y el pronóstico del paciente. Algunos factores que deberían tenerse en cuenta son: el rango de caída de la concentración de hemoglobina, la respuesta a tratamiento con hierro, el riesgo de necesitar transfusión y los riesgos relacionados a los tratamientos con AEE.
5. Darbepoetina alfa versus epoetina alfa
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
Para personas con ERC y anemia recomendamos utilizar la eritropoyetina disponible (epoetina alfa) para el tratamiento de la anemia, evaluando previamente el estado del paciente y la ruta de administración. (Recomendación fuerte a favor)
6. Administración de epoetina alfa
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
En pacientes con ERC que requieran la administración de epoetina alfa, sugerimos usar la vía subcutánea o intravenosa. (Recomendación débil a favor, certeza baja de la evidencia)
BPC 1:
Considerar administrar epoetina alfa por vía intravenosa en pacientes en hemodiálisis, y administrala por vía subcutánea en pacientes que no están en hemodiálisis.
BPC 2:
Cuando se use la vía intravenosa, considerar un ajuste de dosis mayor.
7. Dosis de epoetina alfa
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
En personas con ERC y anemia, en tratamiento con epoetina alfa, recomendamos mantener una dosis promedio de epoetina menor a 10000 unidades/semana. (Recomendación fuerte a favor)
Recomendación 2:
En personas con ERC en prediálisis y anemia, sugerimos administrar la epoetina alfa con una frecuencia de dosis de una vez por semana o una vez cada dos semanas, valorando la severidad de la anemia del paciente. (Recomendación débil a favor)
8. Nivel objetivo de hemoglobina a alcanzar
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
En personas con ERC y anemia, recomendamos mantener una Hb objetivo entre 10.0 y 12.0 g/dL. (Recomendación fuerte a favor)
BPC 1:
Para mantener el nivel de Hb dentro del rango objetivo, no espere hasta que los niveles de Hb estén por debajo del objetivo terapéutico, para ajustar el tratamiento. Se debe ajustar el tratamiento cuando los niveles de Hb alcancen un valor 0.5 g/dL mayor al objetivo terapéutico.
BPC 2:
Evalúe aceptar niveles de Hb debajo de los objetivos terapéuticos si se requiere altas dosis de epoetina alfa para alcanzar los niveles objetivo, o si no alcanza niveles objetivo, a pesar de administrar una dosis mayor.
9. Sospecha de resistencia a los AEE
Descargar PDF con el desarrollo de la pregunta.
BPC 1:
En personas con ERC y anemia en tratamiento con AEE, sospechar de resistencia a los AEE si:
- Se han investigado otras causas de anemia (desnutrición, hiperparatiroidismo, inflamación crónica, infección, pérdida sanguínea, neoplasia, diálisis inadecuada, toxicidad por aluminio), y
- No se alcanza el nivel objetivo de Hb a pesar del tratamiento con 300 UI/Kg/semana o más de epoetina subcutánea, o 450 UI/Kg/semana o más de epoetina endovenosa; o existe una necesidad continua de administrar AEE
10. Transfusiones de sangre
Descargar PDF con el desarrollo de la pregunta.
BPC 1:
Evaluar y discutir los riesgos y beneficios de la transfusión de glóbulos rojos con el paciente (o, cuando corresponda, con sus familiares o cuidadores).
BPC 2:
Considerar la indicación de transfusión sanguínea cuando:
- Se requiere una rápida corrección de la anemia para estabilizar la condición del paciente (por ejemplo, en casos de hemorragia aguda o isquemia miocárdica inestable) o es necesario corregir rápidamente la Hb para una cirugía.
- Persisten los síntomas y signos de anemia, con respuesta ineficaz a la terapia con AEE.
Los riesgos de administrar AEE superan los riesgos de transfusión de sangre.
BPC 3:
Evitar, en lo posible, corregir la anemia con transfusiones de sangre en personas con ERC candidatos a trasplante renal.
BPC 4:
De decidir realizar transfusiones de sangre en personas con ERC candidatos a trasplante renal, utilizar el filtro leucorreductor.
Referencias bibliográficas
- Francis ER, Kuo C-C, Bernabe-Ortiz A, Nessel L, Gilman RH, Checkley W, et al. Burden of chronic kidney disease in resource-limited settings from Peru: a population-based study. BMC nephrology. 2015;16(1).
- Cameron J. European best practice guidelines for the management of anaemia in patients with chronic renal failure. Nephrology, dialysis, transplantation: official publication of the European Dialysis and Transplant Association-European Renal Association. 1999;14(suppl_2):61-5.
- Thorp ML, Johnson ES, Yang X, Petrik AF, Platt R, Smith DH. Effect of anaemia on mortality, cardiovascular hospitalizations and end‐stage renal disease among patients with chronic kidney disease. Nephrology. 2009;14(2):240-6.
- MINSA. Metodología para la elaboración de Guías de Práctica Clínica. In: Pública DGdS, editor. Lima-Peru: Ministerio de Salud; 2015. p. 1-53.
- ESSALUD. Directiva para el Desarrollo de Guias de Practica Clinica en EsSalud. In: IETSI, editor. Lima- Perú: EsSalud; 2016. p. 1-30.
- NICE. Anemia management in chronic kidney disease. New England: NICE; 2015.
- KDIGO. Clinical Practice Guideline for Anemia in chronic kidney disease. KDIGO; 2012. p. 1-64.
- Andrews JC, Schünemann HJ, Oxman AD, Pottie K, Meerpohl JJ, Coello PA, et al. GRADE guidelines: 15. Going from evidence to recommendation—determinants of a recommendation’s direction and strength. Journal of clinical epidemiology. 2013;66(7):726-35.
- Higgins JP, Altman DG, Gøtzsche PC, Jüni P, Moher D, Oxman AD, et al. The Cochrane Collaboration’s tool for assessing risk of bias in randomised trials. Bmj. 2011;343:d5928.
- Shea BJ, Grimshaw JM, Wells GA, Boers M, Andersson N, Hamel C, et al. Development of AMSTAR: a measurement tool to assess the methodological quality of systematic reviews. BMC medical research methodology. 2007;7:10.
- Stang A. Critical evaluation of the Newcastle-Ottawa scale for the assessment of the quality of nonrandomized studies in meta-analyses. European journal of epidemiology. 2010;25(9):603-5.
- Ministerio de Salud. Documento técnico: Metodología para la de documento técnico elaboración guías de practica clínica. Lima, Perú: MINSA; 2015.
- Collaboration A. The ADAPTE process: resource toolkit for guideline adaptation. Version 2.0. Available at:)(Accessed November 13, 2014). 2009.
- Andrews J, Guyatt G, Oxman AD, Alderson P, Dahm P, Falck-Ytter Y, et al. GRADE guidelines: 14. Going from evidence to recommendations: the significance and presentation of recommendations. Journal of clinical epidemiology. 2013;66(7):719-25.
- Kuragano T, Matsumura O, Matsuda A, Hara T, Kiyomoto H, Murata T, et al. Association between hemoglobin variability, serum ferritin levels, and adverse events/mortality in maintenance hemodialysis patients. Kidney international. 2014;86(4):845-54.
- Ueda N, Takasawa K. Role of Hepcidin-25 in Chronic Kidney Disease: Anemia and Beyond. Current medicinal chemistry. 2017;24(14):1417-52.
- Astor BC, Muntner P, Levin A, Eustace JA, Coresh J. Association of kidney function with anemia: the Third National Health and Nutrition Examination Survey (1988-1994). Archives of internal medicine. 2002;162(12):1401-8.
- Kazmi WH, Kausz AT, Khan S, Abichandani R, Ruthazer R, Obrador GT, et al. Anemia: an early complication of chronic renal insufficiency. American Journal of Kidney Diseases. 2001;38(4):803-12.
- Han SY, Oh SW, Hong JW, Yi SY, Noh JH, Lee HR, et al. Association of Estimated Glomerular Filtration Rate with Hemoglobin Level in Korean Adults: The 2010–2012 Korea National Health and Nutrition Examination Survey. PloS one. 2016;11(4):e0150029.
- Organization WH. Iron Deficiency Anaemia Assesment, Prevention and Control. World Health Organization; 2001.
- INEI. Censos Nacionales 2007: XI Población y VI de Vivienda. Capítulo 1: Características de la población . Perfil sociodemográfico del Perú 2007. . Lima-Perú: INEI; 2008.
- Hurtado Alberto MC, Delgado Ernesto. Infuence of anoxemia on the hemopoietic activity. Archives of internal medicine. 1945;75:284-323.
- Kitsati N, Liakos D, Ermeidi E, Mantzaris MD, Vasakos S, Kyratzopoulou E, et al. Rapid elevation of transferrin saturation and serum hepcidin concentration in hemodialysis patients after intravenous iron infusion. Haematologica. 2015;100(3):e80-3.
- Tessitore N, Solero GP, Lippi G, Bassi A, Faccini GB, Bedogna V, et al. The role of iron status markers in predicting response to intravenous iron in haemodialysis patients on maintenance erythropoietin. Nephrology Dialysis Transplantation. 2001;16(7):1416-23.
- Ahluwalia N, Skikne BS, Savin V, Chonko A. Markers of masked iron deficiency and effectiveness of EPO therapy in chronic renal failure. American journal of kidney diseases. 1997;30(4):532-41.
- Bovy C, Gothot A, Delanaye P, Warling X, Krzesinski J-M, Beguin Y. Mature erythrocyte parameters as new markers of functional iron deficiency in haemodialysis: sensitivity and specificity. Nephrology Dialysis Transplantation. 2007;22(4):1156-62.
- Buttarello M, Pajola R, Novello E, Rebeschini M, Cantaro S, Oliosi F, et al. Diagnosis of iron deficiency in patients undergoing hemodialysis. American journal of clinical pathology. 2010;133(6):949-54.
- Chen Y-C, Hung S-C, Tarng D-C. Association between transferrin receptor–ferritin index and conventional measures of iron responsiveness in hemodialysis patients. American journal of kidney diseases. 2006;47(6):1036-44.
- Domrongkitchaiporn S, Jirakranont B, Atamasrikul K, Ungkanont A, Bunyaratvej A. Indices of iron status in continuous ambulatory peritoneal dialysis patients. American journal of kidney diseases. 1999;34(1):29-35.
- Fishbane S, Galgano C, Langley RC, Canfield W, Maesaka JK. Reticulocyte hemoglobin content in the evaluation of iron status of hemodialysis patients. Kidney international. 1997;52(1):217-22.
- Fishbane S, Kowalski EA, Imbriano LJ, Maesaka JK. The evaluation of iron status in hemodialysis patients. Journal of the American Society of Nephrology. 1996;7(12):2654-7.
- Fishbane S, Shapiro W, Dutka P, Valenzuela OF, Faubert J. A randomized trial of iron deficiency testing strategies in hemodialysis patients. Kidney international. 2001;60(6):2406-11.
- Kaneko Y, Miyazaki S, Hirasawa Y, Gejyo F, Suzuki M. Transferrin saturation versus reticulocyte hemoglobin content for iron deficiency in Japanese hemodialysis patients. Kidney international. 2003;63(3):1086-93.
- Stancu S, Bârsan L, Stanciu A, Mircescu G. Can the response to iron therapy be predicted in anemic nondialysis patients with chronic kidney disease? Clinical Journal of the American Society of Nephrology. 2010;5(3):409-16.
- Chand S, Ward DG, Ng ZY, Hodson J, Kirby H, Steele P, et al. Serum hepcidin-25 and response to intravenous iron in patients with non-dialysis chronic kidney disease. Journal of nephrology. 2015;28(1):81-8.
- Archer NM, Brugnara C. Diagnosis of iron-deficient states. Critical reviews in clinical laboratory sciences. 2015;52(5):256-72.
- Wittwer I. Iron deficiency anaemia in chronic kidney disease. Journal of renal care. 2013;39(3):182-8.
- Agarwal R, Rizkala AR, Bastani B, Kaskas MO, Leehey DJ, Besarab A. A randomized controlled trial of oral versus intravenous iron in chronic kidney disease. American journal of nephrology. 2006;26(5):445-54.
- Fudin R, Jaichenko J, Shostak A, Bennett M, Gotloib L. Correction of uremic iron deficiency anemia in hemodialyzed patients: a prospective study. Nephron. 1998;79(3):299-305.
- Macdougall IC, Bock AH, Carrera F, Eckardt KU, Gaillard C, Van Wyck D, et al. FIND-CKD: a randomized trial of intravenous ferric carboxymaltose versus oral iron in patients with chronic kidney disease and iron deficiency anaemia. Nephrology, dialysis, transplantation : official publication of the European Dialysis and Transplant Association – European Renal Association. 2014;29(11):2075-84.
- Qunibi WY, Martinez C, Smith M, Benjamin J, Mangione A, Roger SD. A randomized controlled trial comparing intravenous ferric carboxymaltose with oral iron for treatment of iron deficiency anaemia of non-dialysis-dependent chronic kidney disease patients. Nephrology Dialysis Transplantation. 2010;26(5):1599-607.
- Sheashaa H, El-Husseini A, Sabry A, Hassan N, Salem A, Khalil A, et al. Parenteral iron therapy in treatment of anemia in end-stage renal disease patients: a comparative study between iron saccharate and gluconate. Nephron. 2005;99(4):c97.
- Spinowitz BS, Kausz AT, Baptista J, Noble SD, Sothinathan R, Bernardo MV, et al. Ferumoxytol for treating iron deficiency anemia in CKD. Journal of the American Society of Nephrology. 2008;19(8):1599-605.
- Tonelli M, Winkelmayer WC, Jindal KK, Owen WF, Manns BJ. The cost-effectiveness of maintaining higher hemoglobin targets with erythropoietin in hemodialysis patients. Kidney international. 2003;64(1):295-304.
- Adhikary L, Acharya S. Efficacy of IV Iron Compared to Oral Iron for Increment of Haemoglobin Level in Anemic Chronic Kidney Disease Patients. Journal of Nepal Medical Association. 2011;51(183).
- Charytan C, Qunibi W, Bailie GR. Comparison of intravenous iron sucrose to oral iron in the treatment of anemic patients with chronic kidney disease not on dialysis. Nephron Clinical Practice. 2005;100(3):c55-c62.
- Coyne DW, Kapoian T, Suki W, Singh AK, Moran JE, Dahl NV, et al. Ferric gluconate is highly efficacious in anemic hemodialysis patients with high serum ferritin and low transferrin saturation: results of the Dialysis Patients’ Response to IV Iron with Elevated Ferritin (DRIVE) Study. Journal of the American Society of Nephrology. 2007;18(3):975-84.
- Li H, Wang S-x. Intravenous iron sucrose in Chinese hemodialysis patients with renal anemia. Blood purification. 2008;26(2):151-6.
- Li H, Wang S-X. Intravenous iron sucrose in peritoneal dialysis patients with renal anemia. Peritoneal Dialysis International. 2008;28(2):149-54.
- Markowitz G, Kahn G, Feingold R, Coco M, Lynn R. An evaluation of the effectiveness of oral iron therapy in hemodialysis patients receiving recombinant human erythropoietin. Clinical nephrology. 1997;48(1):34-40.
- Provenzano R, Schiller B, Rao M, Coyne D, Brenner L, Pereira BJ. Ferumoxytol as an intravenous iron replacement therapy in hemodialysis patients. Clinical Journal of the American Society of Nephrology. 2009;4(2):386-93.
- Singh H, Reed J, Noble S, Cangiano JL, Van Wyck DB, Group USISCT. Effect of intravenous iron sucrose in peritoneal dialysis patients who receive erythropoiesis-stimulating agents for anemia: a randomized, controlled trial. Clinical Journal of the American Society of Nephrology. 2006;1(3):475-82.
- Stoves J, Inglis H, Newstead CG. A randomized study of oral vs intravenous iron supplementation in patients with progressive renal insufficiency treated with erythropoietin. Nephrology Dialysis Transplantation. 2001;16(5):967-74.
- Qunibi WY, Martinez C, Smith M, Benjamin J, Mangione A, Roger SD. A randomized controlled trial comparing intravenous ferric carboxymaltose with oral iron for treatment of iron deficiency anaemia of non-dialysis-dependent chronic kidney disease patients. Nephrology, dialysis, transplantation : official publication of the European Dialysis and Transplant Association – European Renal Association. 2011;26(5):1599-607.
- Onken JE, Bregman DB, Harrington RA, Morris D, Buerkert J, Hamerski D, et al. Ferric carboxymaltose in patients with iron-deficiency anemia and impaired renal function: the REPAIR-IDA trial. Nephrology Dialysis Transplantation. 2013;29(4):833-42.
- Shepshelovich D, Rozen-Zvi B, Avni T, Gafter U, Gafter-Gvili A. Intravenous Versus Oral Iron Supplementation for the Treatment of Anemia in CKD: An Updated Systematic Review and Meta-analysis. American journal of kidney diseases : the official journal of the National Kidney Foundation. 2016;68(5):677-90.
- Kalra PA, Bhandari S, Saxena S, Agarwal D, Wirtz G, Kletzmayr J, et al. A randomized trial of iron isomaltoside 1000 versus oral iron in non-dialysis-dependent chronic kidney disease patients with anaemia. Nephrology, dialysis, transplantation : official publication of the European Dialysis and Transplant Association – European Renal Association. 2016;31(4):646-55.
- Wong G, Howard K, Hodson E, Irving M, Craig JC. An economic evaluation of intravenous versus oral iron supplementation in people on haemodialysis. Nephrology Dialysis Transplantation. 2012;28(2):413-20.
- Seliger S, Fox KM, Gandra SR, Bradbury B, Hsu VD, Walker L, et al. Timing of erythropoiesis-stimulating agent initiation and adverse outcomes in nondialysis CKD: a propensity-matched observational study. Clinical journal of the American Society of Nephrology : CJASN. 2010;5(5):882-8.
- Evans M, Carrero J-J, Bellocco R, Barany P, Qureshi AR, Seeberger A, et al. Initiation of erythropoiesis-stimulating agents and outcomes: a nationwide observational cohort study in anaemic chronic kidney disease patients. Nephrology Dialysis Transplantation. 2016:gfw328.
- Vinhas J, Barreto C, Assunção J, Parreira L, Vaz A. Treatment of anaemia with erythropoiesis-stimulating agents in patients with chronic kidney disease does not lower mortality and may increase cardiovascular risk: a meta-analysis. Nephron Clinical Practice. 2012;121(3-4):c95-c101.
- Nissenson AR, Swan SK, Lindberg JS, Soroka SD, Beatey R, Wang C, et al. Randomized, controlled trial of darbepoetin alfa for the treatment of anemia in hemodialysis patients. American journal of kidney diseases. 2002;40(1):110-8.
- Palmer SC, Saglimbene V, Mavridis D, Salanti G, Craig JC, Tonelli M, et al. Erythropoiesis-stimulating agents for anaemia in adults with chronic kidney disease: a network meta-analysis. The Cochrane database of systematic reviews. 2014(12):Cd010590.
- Al-Ali FS, El-Sayed Abdelfattah M, Fawzy AA, Hamdy AF, Abdulla AE. Erythropoietin-stimulating agents in the management of anemia of end-stage renal disease patients on regular hemodialysis: a prospective randomized comparative study from Qatar. Hemodialysis international International Symposium on Home Hemodialysis. 2015;19(1):33-43.
- Kaufman JS, Reda DJ, Fye CL, Goldfarb DS, Henderson WG, Kleinman JG, et al. Subcutaneous compared with intravenous epoetin in patients receiving hemodialysis. New England Journal of Medicine. 1998;339(9):578-83.
- Patel T, Hirter A, Kaufman J, Keithi-Reddy SR, Reda D, Singh A. Route of epoetin administration influences hemoglobin variability in hemodialysis patients. American journal of nephrology. 2009;29(6):532-7.
- Koulouridis I, Alfayez M, Trikalinos TA, Balk EM, Jaber BL. Dose of erythropoiesis-stimulating agents and adverse outcomes in CKD: a metaregression analysis. American Journal of Kidney Diseases. 2013;61(1):44-56.
- Hahn D, Esezobor CI, Elserafy N, Webster AC, Hodson EM. Short-acting erythropoiesis-stimulating agents for anaemia in predialysis patients. status and date: New, published in. 2015(5).
- Drueke TB, Barany P, Cazzola M, Eschbach JW, Grutzmacher P, Kaltwasser JP, et al. Management of iron deficiency in renal anemia: guidelines for the optimal therapeutic approach in erythropoietin-treated patients. Clinical nephrology. 1997;48(1):1-8.
- Drueke TB, Locatelli F, Clyne N, Eckardt KU, Macdougall IC, Tsakiris D, et al. Normalization of hemoglobin level in patients with chronic kidney disease and anemia. N Engl J Med. 2006;355(20):2071-84.
- Furuland H, Linde T, Ahlmen J, Christensson A, Strombom U, Danielson BG. A randomized controlled trial of haemoglobin normalization with epoetin alfa in pre-dialysis and dialysis patients. Nephrology, dialysis, transplantation : official publication of the European Dialysis and Transplant Association – European Renal Association. 2003;18(2):353-61.
- Roger SD, McMahon LP, Clarkson A, Disney A, Harris D, Hawley C, et al. Effects of early and late intervention with epoetin alpha on left ventricular mass among patients with chronic kidney disease (stage 3 or 4): results of a randomized clinical trial. Journal of the American Society of Nephrology : JASN. 2004;15(1):148-56.
- Rossert J, Levin A, Roger SD, Horl WH, Fouqueray B, Gassmann-Mayer C, et al. Effect of early correction of anemia on the progression of CKD. American journal of kidney diseases : the official journal of the National Kidney Foundation. 2006;47(5):738-50.
- Pfeffer MA, Burdmann EA, Chen CY, Cooper ME, de Zeeuw D, Eckardt KU, et al. A trial of darbepoetin alfa in type 2 diabetes and chronic kidney disease. N Engl J Med. 2009;361(21):2019-32.
- Singh AK, Szczech L, Tang KL, Barnhart H, Sapp S, Wolfson M, et al. Correction of anemia with epoetin alfa in chronic kidney disease. N Engl J Med. 2006;355(20):2085-98.
- Ritz E, Laville M, Bilous RW, O’Donoghue D, Scherhag A, Burger U, et al. Target level for hemoglobin correction in patients with diabetes and CKD: primary results of the Anemia Correction in Diabetes (ACORD) Study. American journal of kidney diseases : the official journal of the National Kidney Foundation. 2007;49(2):194-207.
- Macdougall IC, Temple RM, Kwan JT. Is early treatment of anaemia with epoetin-alpha beneficial to pre-dialysis chronic kidney disease patients? Results of a multicentre, open-label, prospective, randomized, comparative group trial. Nephrology, dialysis, transplantation : official publication of the European Dialysis and Transplant Association – European Renal Association. 2007;22(3):784-93.
- Collister D, Komenda P, Hiebert B, Gunasekara R, Xu Y, Eng F, et al. The Effect of Erythropoietin-Stimulating Agents on Health-Related Quality of Life in Anemia of Chronic Kidney DiseaseA Systematic Review and Meta-analysisErythropoietin-Stimulating Agents in Anemia of Chronic Kidney Disease. Annals of internal medicine. 2016;164(7):472-8.
- Jing Z, Wei-jie Y, Nan Z, Yi Z, Ling W. Hemoglobin targets for chronic kidney disease patients with anemia: a systematic review and meta-analysis. PloS one. 2012;7(8):e43655.
- Yarnoff BO, Hoerger TJ, Simpson SA, Pavkov ME, Burrows NR, Shrestha SS, et al. The Cost-Effectiveness of Anemia Treatment for Persons with Chronic Kidney Disease. PloS one. 2016;11(7):e0157323.
- European best practice guidelines for the management of anemia in patients with chronic renal failure. SECTION IV. Failure to respond to treatment. Nephrology Dialysis Transplantation. 2004;19(suppl_2):ii32-ii6.
- Eschbach J, Egrie J, Downing M, Browne J, Adamson J. Correction of the anemia of end-stage renal disease with recombinant human erythropoietin. Results of a combined phase I and II clinical trial. The New England journal of medicine. 1987;316(2):73.
- Eschbach JW, Abdulhadi MH, Browne JK, Delano BG, Downing MR, Egrie JC, et al. Recombinant human erythropoietin in anemic patients with end-stage renal disease: results of a phase III multicenter clinical trial. Annals of internal medicine. 1989;111(12):992-1000.
- Casadevall N. Pure red cell aplasia and anti-erythropoietin antibodies in patients treated with epoetin. Nephrology Dialysis Transplantation. 2003;18(suppl_8):viii37-viii41.
- Tarng D-C, Huang T-P. Recombinant human erythropoietin resistance in iron-replete hemodialysis patients: role of aluminum toxicity. American journal of nephrology. 1998;18(1):1-8.
- Kimachi M, Fukuma S, Yamazaki S, Yamamoto Y, Akizawa T, Akiba T, et al. Minor Elevation in C-Reactive Protein Levels Predicts Incidence of Erythropoiesis-Stimulating Agent Hyporesponsiveness among Hemodialysis Patients. Nephron. 2015;131(2):123-30.
- Rubab Z, Amin H, Abbas K, Hussain S, Ullah MI, Mohsin S. Serum hepcidin levels in patients with end-stage renal disease on hemodialysis. Saudi journal of kidney diseases and transplantation : an official publication of the Saudi Center for Organ Transplantation, Saudi Arabia. 2015;26(1):19-25.
- Crowley J, Valeri C, Metzger J, Pono L, Chazan J. Lymphocyte subpopulations in long‐term dialysis patients: a case‐controlled study of the effects of blood transfusion. Transfusion. 1990;30(7):644-7.
- d’Apice AJ, Tait BD. An elective transfusion policy: sensitization rates, patient transplantability, and transplant outcome. Transplantation. 1982;33(2):191-5.
- Balasubramaniam GS, Morris M, Gupta A, Mesa IR, Thuraisingham R, Ashman N. Allosensitization rate of male patients awaiting first kidney grafts after leuko-depleted blood transfusion. Transplantation. 2012;93(4):418-22.
- Collins AJ, Foley RN, Gilbertson DT, Chen SC. United States Renal Data System public health surveillance of chronic kidney disease and end-stage renal disease. Kidney international supplements. 2015;5(1):2-7.
- Gill KS, Muntner P, Lafayette RA, Petersen J, Fink JC, Gilbertson DT, et al. Red blood cell transfusion use in patients with chronic kidney disease. Nephrology, dialysis, transplantation : official publication of the European Dialysis and Transplant Association – European Renal Association. 2013;28(6):1504-15.
- Gill K, Fink JC, Gilbertson DT, Monda KL, Muntner P, Lafayette RA, et al. Red blood cell transfusion, hyperkalemia, and heart failure in advanced chronic kidney disease. Pharmacoepidemiology and drug safety. 2015;24(6):654-62.
- EsSalud. Manual para la obtención, procesamiento, suministro y uso racional de la sangre y sus hemocomponentes en EsSalud. In: Central G, editor. Lima-Perú: EsSaalud; 2000. p. 1-22.
Si tienes comentarios sobre el contenido de las guías de práctica clínica, puedes comunicarte con IETSI-EsSalud enviando un correo: gpcdireccion.ietsi@essalud.gob.pe

SUGERENCIAS
Si has encontrado un error en esta página web o tienes alguna sugerencia para su mejora, puedes comunicarte con EviSalud enviando un correo a evisalud@gmail.com

