DESCARGAR
VERSIÓN EXTENSA
DESCARGAR
ANEXOS
DESCARGAR
VERSIÓN CORTA
DESCARGAR RECOMENDACIONES Y FLUJOGRAMAS
vacio
vacio
Ámbito
•El ámbito asistencial incluye los servicios o unidades de emergencia, servicios o unidades de cardiología, pediatría, cirugía cardiovascular y hemodinamia, en establecimientos de salud del III nivel de atención con capacidad resolutiva, de EsSalud.
Población y alcance
•Pacientes menores de 18 años con comunicación interventricular.
Autores
Grupo elaborador
Expertos clínicos:
- Antonio Ángel Skrabonja Crespo
Médico especialista en Cardiología y Cardiología Infantil, Instituto Nacional Cardiovascular “Carlos Alberto Peschiera Carrillo”, EsSalud, Lima, Perú - Karina Elena Culqui Lévano
Médica especialista en Pediatría y Cardiología Infantil, Hospital Nacional Alberto Sabogal Sologuren, EsSalud, Lima, Perú - Neri Nohemí Taipe Quispe
Médica especialista en Cirugía Torácica y Cardiovascular, Hospital Nacional Edgardo Rebagliati Martins, EsSalud, Lima, Perú - Juan Carlo Zúñiga Meza
Médico especialista en Pediatría y Cardiología Infantil, Instituto Nacional Cardiovascular “Carlos Alberto Peschiera Carrillo”, EsSalud, Lima, Perú - Iván Niño de Guzmán León
Médico especialista en Cirugía Torácica y Cardiovascular, Instituto Nacional Cardiovascular “Carlos Alberto Peschiera Carrillo”, EsSalud, Lima, Perú - Pedro Iván Rojas Sánchez
Médico especialista en Cirugía de Tórax y Cardiovascular, Hospital Nacional Alberto Sabogal Sologuren, EsSalud, Lima, Perú - Joely Carmen Frisancho Berrios
Médica especialista en Pediatría y Cardiología Pediátrica, Instituto Nacional Cardiovascular “Carlos Alberto Peschiera Carrillo”, EsSalud, Lima, Perú - Cindy Pilar Vásquez Marzano
Médica especialista en Cirugía Torácica y Cardiovascular, Hospital Nacional Edgardo Rebagliati Martins, EsSalud, Lima, Perú
Metodólogos:
- Oscar Orlando Rivera Torrejón
Metodólogo, IETSI, EsSalud, Lima, Perú - Mario Enrique Díaz Barrera
Metodólogo, IETSI, EsSalud, Lima, Perú - Lelis Gabriela Coronel Chucos
Metodóloga, IETSI, EsSalud, Lima, Perú
Coordinadoras del grupo elaborador:
- Joan Caballero Luna
IETSI, EsSalud, Lima, Perú - Fabiola Mercedes Huaroto Ramírez
IETSI, EsSalud, Lima, Perú
Metodología
Resumen de la metodología:
- Conformación del GEG: La Dirección de Guías de Práctica Clínica, Farmacovigilancia y Tecnovigilancia, del Instituto de Evaluación de Tecnologías en Salud e Investigación (IETSI) del Seguro Social del Perú (EsSalud), conformó un grupo elaborador de la guía (GEG), que incluyó médicos especialistas y metodólogos.
- Planteamiento de preguntas clínicas: En concordancia con los objetivos y alcances de esta GPC, se formularon las preguntas clínicas.
- Búsqueda de la evidencia para cada pregunta: Para cada pregunta clínica, se realizaron búsquedas de revisiones sistemáticas (publicadas como artículos científicos o guías de práctica clínica). De no encontrar revisiones de calidad, se buscaron estudios primarios, cuyo riesgo de sesgo fue evaluado usando herramientas estandarizadas.
- Evaluación de la certeza de la evidencia: Para graduar la certeza de la evidencia, se siguió la metodología Grading of Recommendations Assessment, Development, and Evaluation (GRADE), y se usaron tablas de Summary of Findings (SoF).
- Formulación de las recomendaciones: El GEG revisó la evidencia recolectada para cada una de las preguntas clínicas en reuniones periódicas, en las que formuló las recomendaciones usando la metodología GRADE, otorgándole una fuerza a cada una. Para ello, se tuvo en consideración los beneficios y daños de las opciones, valores y preferencias de los pacientes, aceptabilidad, factibilidad, equidad y uso de recursos. Estos criterios fueron presentados y discutidos, tomando una decisión por consenso o mayoría simple. Asimismo, el GEG emitió puntos de buenas prácticas clínicas (BPC) sin una evaluación formal de la evidencia, y mayormente en base a su experiencia clínica.
- Revisión externa: La presente GPC fue revisada en reuniones con profesionales representantes de otras instituciones, tomadores de decisiones, y expertos externos.
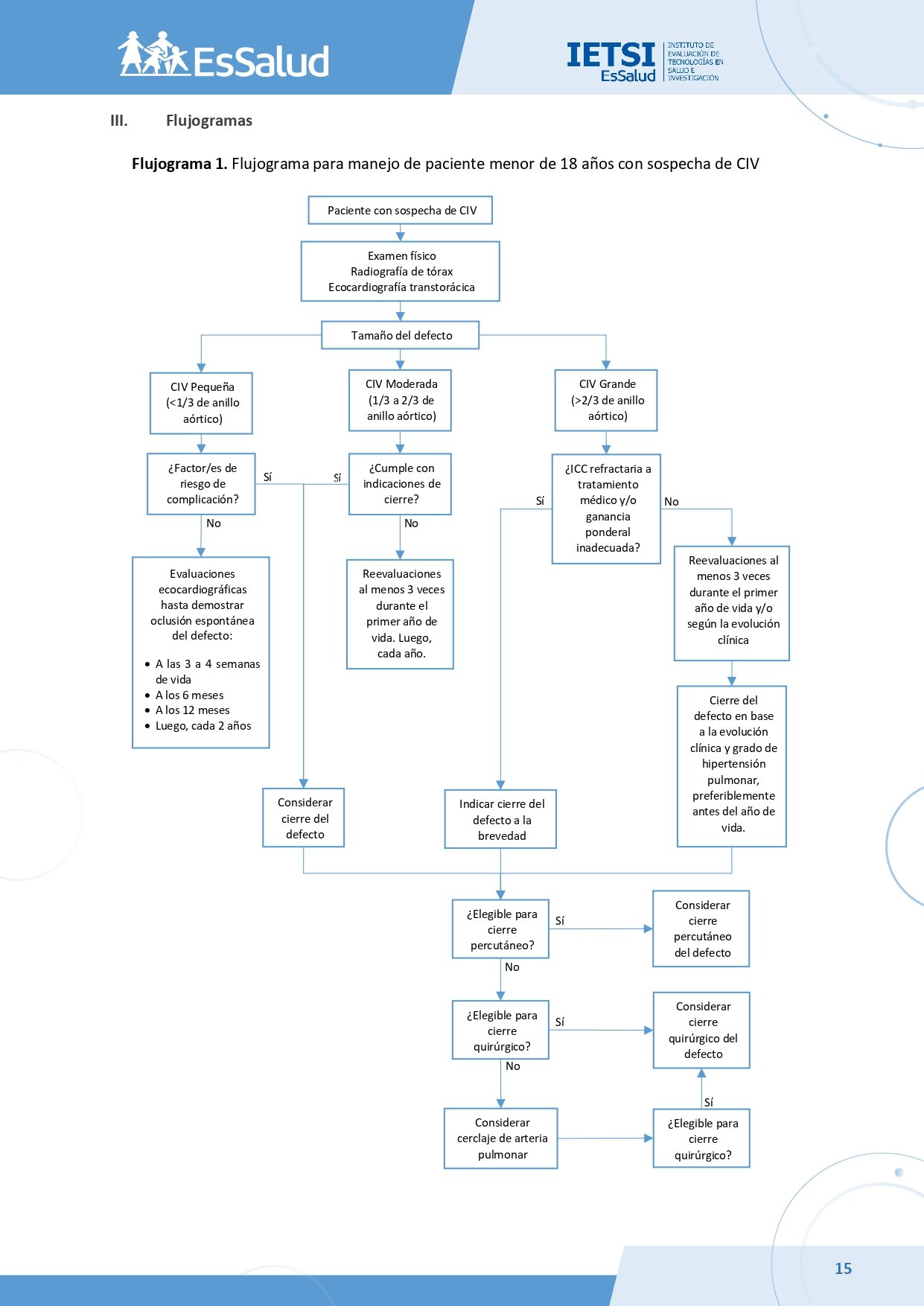
Flujogramas que resumen el contenido de la GPC
vacio
vacio
1. Cierre del defecto en CIV pequeña
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
En pacientes menores de 18 años con CIV pequeña (tamaño menor a 1/3 del tamaño del anillo aórtico), considerar el cierre del defecto cuando el paciente presente cualquiera de las siguientes condiciones:
- Endocarditis infecciosa activa o antecedente de endocarditis infecciosa.
- Prolapso de velo aórtico con regurgitación progresiva.
- CIV asociada a otra patología cardíaca que requiera intervención quirúrgica.
- CIV de salida (supracristal, subpulmonar o doblemente relacionado).
- Valor de Qp/Qs > 1.5, repercusión hemodinámica, cardiomegalia en radiografía de tórax o clínica de insuficiencia cardíaca (ICC).
(BPC)
Recomendación 2:
En pacientes menores de 18 años con CIV pequeña, realizar reevaluaciones que busquen la presencia de indicaciones de cierre del defecto e incluyan una evaluación ecocardiográfica. Estas reevaluaciones deben realizarse hasta demostrarse la oclusión espontánea del defecto.
- A las 3 a 4 semanas de edad.
- A los 6 meses de edad.
- A los 12 meses de edad.
- Posteriormente, cada 2 años.
(BPC)
2. Cierre del defecto en CIV moderada
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
En pacientes con una CIV moderada (tamaño entre 1/3 a 2/3 del tamaño del anillo aórtico), considerar las siguientes indicaciones para cierre:
- Persistencia de síntomas a pesar de un tratamiento médico adecuado.
- Aumento de la presión pulmonar o signos indirectos de aumento de la presión pulmonar (considerar cierre preferiblemente dentro del primer año de vida).
- Defectos subpulmonares y membranosos, con prolapso de válvula aórtica y regurgitación aórtica asociada.
- Repercusión hemodinámica (Qp/Qs > 2, dilatación de cavidades cardiacas, cardiomegalia en radiografía de tórax y/o signos de ICC).
- CIV asociada a otra patología cardíaca que requiera intervención quirúrgica.
(BPC)
Recomendación 2:
En pacientes menores de 18 años con CIV moderada, la reevaluación por Cardiología debe realizarse al menos tres veces durante el primer año de vida, buscando indicaciones para cierre.
(BPC)
Recomendación 3:
Si pasado el año de vida, el paciente menor de 18 años con CIV moderada persiste asintomático y sin indicaciones para cierre, mantener los controles por Cardiología con electrocardiografía y ecocardiografía cada año o adelantarlo ante la sospecha de obstrucción de tracto de salida o insuficiencia aórtica.
Si en los controles se evidencia cierre espontáneo del defecto, realizar un control adicional al año para considerar el alta bajo criterio médico.
(BPC)
3. Cierre del defecto en CIV grande
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
En pacientes menores de 18 años con una CIV grande (tamaño mayor a 2/3 del tamaño del anillo aórtico), realizar el cierre del defecto en base a la evolución clínica y grado de hipertensión pulmonar, preferiblemente antes del año de vida.
(BPC)
Recomendación 2:
En pacientes menores de 18 años con una CIV grande con insuficiencia cardíaca refractaria a tratamiento médico y/o ganancia ponderal inadecuada, indicar el cierre del defecto a la brevedad.
- Se define ganancia ponderal inadecuada como una caída en el percentil peso/edad, peso/talla o talla/edad.
(BPC)
Recomendación 3:
En pacientes con una CIV grande no cerrada con evolución favorable, realizar reevaluaciones clínicas y ecocardiográficas al menos cada 3 meses durante el primer año de vida y/o según la evolución clínica.
(BPC)
4. Cierre percutáneo o quirúrgico
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
En menores de 18 años con diagnóstico de CIV perimembranosa con indicación de cierre, sugerimos brindar el cierre percutáneo, según criterios de elegibilidad, en lugar de cierre quirúrgico.
Consideración: Los criterios de elegibilidad para el cierre percutáneo incluyen:
- Peso > 10 kg.
- Cortocircuito de izquierda a derecha.
- Valor Qp/Qs > 1.5.
- Cardiomegalia o dilatación de cavidades izquierdas.
- Ganancia ponderal inadecuada.
- Progresión de clase funcional según la clasificación de Ross.
- Infecciones respiratorias recurrentes.
- Antecedente de endocarditis infecciosa.
(BPC)
Recomendación 2:
Las contraindicaciones para el cierre percutáneo en pacientes menores de 18 años con CIV perimembranosa e indicación de cierre son las siguientes:
- CIV con enfermedad vascular pulmonar irreversible (RVP > 8UW/m²).
- Bloqueo de rama izquierda preexistente o bloqueo auriculoventricular de segundo o tercer grado.
- Cualquier regurgitación aórtica.
- Lesiones asociadas intracardíacas que requieran reparación quirúrgica.
- Contraindicaciones para terapia antiagregante plaquetaria.
- Infección activa o sepsis.
- Anatomía incompatible, como tamaño del defecto efectivo > 10 mm o distancia < 4 mm del CIV al anillo aórtico.
(BPC)
Recomendación 1:
En pacientes menores de 18 años con diagnóstico de CIV muscular con indicación de cierre, se puede elegir el cierre percutáneo, según criterios de elegibilidad, en lugar de cierre quirúrgico.
Consideración: Los criterios de elegibilidad para el cierre percutáneo incluyen:
- Peso > 8 kg.
- Cortocircuito de izquierda a derecha.
- Valor Qp/Qs > 1.5.
- Cardiomegalia o dilatación de cavidades izquierdas.
- Ganancia ponderal inadecuada.
- Progresión de clase funcional según la clasificación de Ross.
- Infecciones respiratorias recurrentes.
- Antecedente de endocarditis infecciosa.
(BPC)
Recomendación 2:
Las contraindicaciones para el cierre percutáneo en pacientes menores de 18 años con CIV muscular son las siguientes:
- CIV con enfermedad vascular pulmonar irreversible (RVP > 8UW/m²).
- Bloqueo de rama izquierda preexistente o bloqueo auriculoventricular de segundo o tercer grado.
- Lesiones asociadas intracardíacas que requieran reparación quirúrgica.
- Contraindicaciones para terapia antiagregante plaquetaria.
- Infección activa o sepsis.
- Defectos con un tamaño > 10 mm.
(BPC)
5. Cateterismo cardíaco ante sospecha de HTP
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
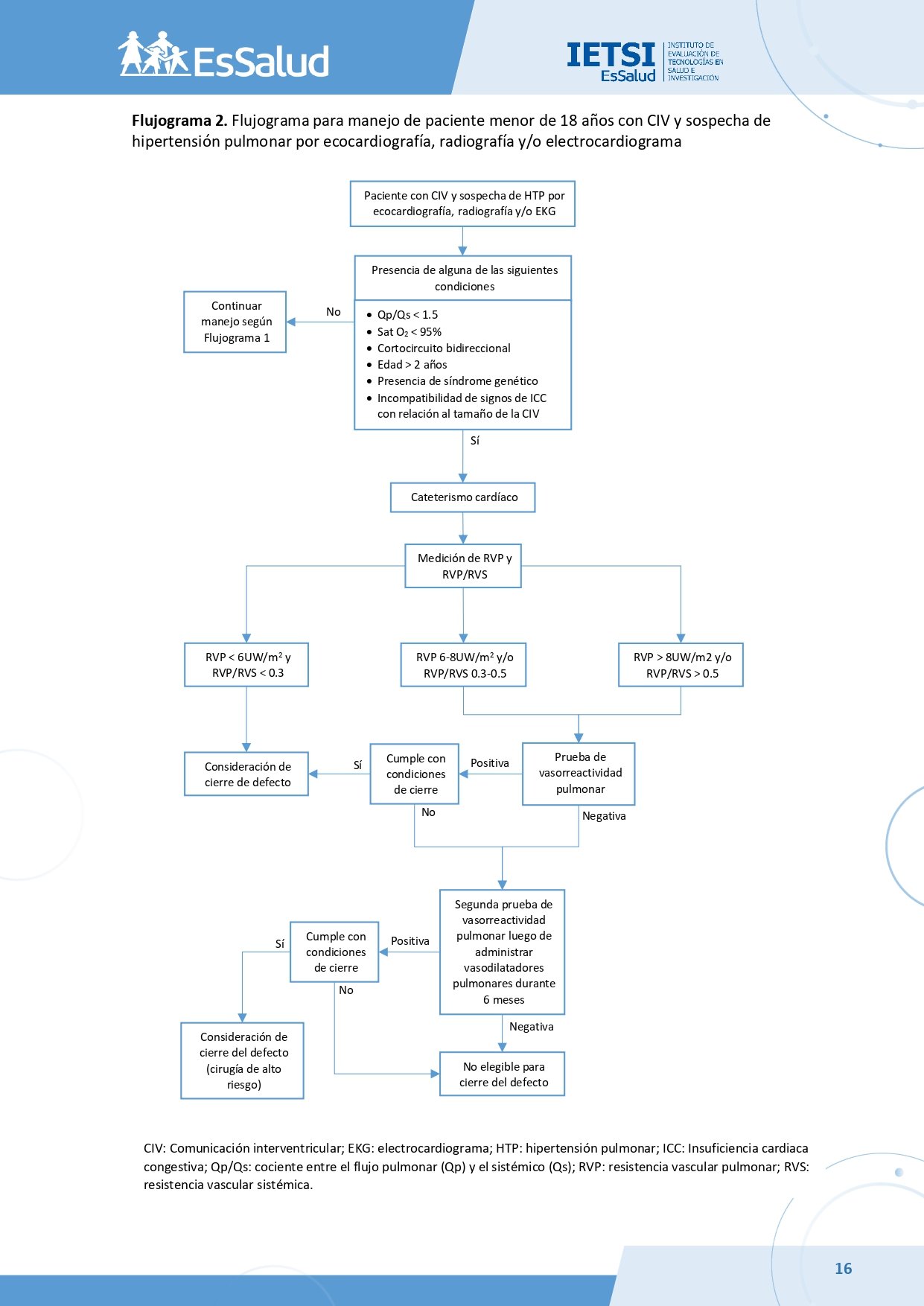
En pacientes menores de 18 años con CIV y sospecha de HTP por ecocardiografía, radiografía y/o EKG, realizar cateterismo cardíaco para obtener la resistencia vascular pulmonar (RVP) cuando se cumpla con alguno de los siguientes criterios:
- Qp/Qs < 1.5.
- Saturación de oxígeno < 95%.
- Cortocircuito bidireccional.
- Edad > 2 años.
- Presencia de síndrome genético.
- Incompatibilidad de signos de insuficiencia cardíaca con relación al tamaño de la CIV.
De lo contrario, considerar el cierre del defecto de acuerdo con lo establecido en la presente GPC.
(BPC)
6. Prueba de vasorreactividad pulmonar
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
En pacientes menores de 18 años con CIV e HTP, proceder de acuerdo con los valores obtenidos de RVP y resistencia vascular sistémica (RVS) de la siguiente manera:
- Zona operable: Indicación de cierre del defecto; la prueba de vasorreactividad pulmonar es opcional.
- Zona gris y zona crítica: La prueba de vasorreactividad pulmonar es necesaria antes de evaluar la posibilidad del cierre del defecto.
Consideración: Clasificación según valores obtenidos:
- Zona operable: RVP < 6UW/m² y RVP/RVS < 0.3.
- Zona gris: RVP 6 a 8 UW/m² y/o RVP/RVS 0.3 a 0.5.
- Zona crítica: RVP > 8UW/m² y/o RVP/RVS > 0.5.
(BPC)
Recomendación 2:
En pacientes menores de 18 años con CIV, hipertensión arterial pulmonar y una prueba de vasorreactividad pulmonar positiva, considerarlos como elegibles para el cierre del defecto si cumplen con las siguientes condiciones:
- Saturación de oxígeno > 95%.
- Qp/Qs > 1.5.
- Clínica de insuficiencia cardíaca.
- Cortocircuito de izquierda a derecha.
- RVP < 8UW/m².
De no cumplir con estas condiciones, considerar la prueba como negativa y continuar manejo según la GPC.
(BPC)
7. Segunda prueba ante primera prueba negativa
Descargar PDF con el desarrollo de la pregunta.
Recomendación 1:
En pacientes menores de 18 años con CIV e hipertensión arterial pulmonar con una primera prueba de vasorreactividad pulmonar negativa, considerar realizar una segunda prueba de vasorreactividad pulmonar luego de un tratamiento previo con vasodilatadores pulmonares durante 6 meses.
(BPC)
Recomendación 2:
En pacientes menores de 18 años con CIV, hipertensión arterial pulmonar y con una segunda prueba de vasorreactividad pulmonar negativa, considerarlos no elegibles para cierre del defecto.
(BPC)
Recomendación 3:
En pacientes menores de 18 años con CIV e hipertensión arterial pulmonar que en una segunda prueba de vasorreactividad pulmonar obtienen un resultado positivo, considerarlos como elegibles para cierre parcial o total del defecto si cumplen con las siguientes condiciones:
- Saturación de oxígeno > 95%.
- Qp/Qs > 1.5.
- Clínica de insuficiencia cardíaca.
- Cortocircuito de izquierda a derecha.
- RVP < 8UW/m².
Consideración: Esta cirugía debe considerarse de alto riesgo.
(BPC)
Referencias bibliográficas
1. Ammash NM. Ventricular Septal Defect. En: Warnes CA, editor. Adult Congenital Heart Disease [Internet]. 1a ed. Wiley; 2009 [citado el 3 de noviembre de 2024]. p. 41–56. Disponible en: https://onlinelibrary.wiley.com/doi/10.1002/9781444311846.ch4
2. Zimmerman MS, Smith AGC, Sable CA, Echko MM, Wilner LB, Olsen HE, et al. Global, regional, and national burden of congenital heart disease, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet Child Adolesc Health. el 1 de marzo de 2020;4(3):185–200.
3. Warnes CA. Adult congenital heart disease: the challenges of a lifetime. Eur Heart J. el 1 de julio de 2017;38(26):2041–7.
4. Malo C, Insa A. Comunicación interventricular. En: Protocolos diagnósticos y terapéuticos en cardiología pediátrica. Valencia; 2015.
5. Roguin N, Du ZD, Barak M, Nasser N, Hershkowitz S, Milgram E. High prevalence of muscular ventricular septal defect in neonates. J Am Coll Cardiol. el 15 de noviembre de 1995;26(6):1545–8.
6. Miyake T, Shinohara T, Inoue T, Marutani S, Takemura T. Spontaneous closure of muscular trabecular ventricular septal defect: comparison of defect positions. Acta Paediatr Oslo Nor 1992. octubre de 2011;100(10):e158-162.
7. Ramaciotti C, Keren A, Silverman NH. Importance of (perimembranous) ventricular septal aneurysm in the natural history of isolated perimembranous ventricular septal defect. Am J Cardiol. el 1 de febrero de 1986;57(4):268–72.
8. Rutledge J, Bricker JT. Congenital Diseases of the Heart: Clinical-Physiological Considerations (Fully Revised and Updated Second Edition). Tex Heart Inst J. 2001;28(3):237.
9. Gumbiner C, Takao A. The Science and Practice of Pediatric Cardiology. 2da ed. Baltimore: Williams & Wilkins; 1998. 1119 p.
10. CENETEC. Diagnóstico y tratamiento de los defectos de los tabiques interauricular e interventricular en menores de 18 años en segundo y tercer nivel de atención. Guía de evidencias y recomendaciones: Guía de práctica clínica. México; 2018.
11. Saxena A, Relan J, Agarwal R, Awasthy N, Azad S, Chakrabarty M, et al. Indian Guidelines for Indications and Timing of Intervention for Common Congenital Heart Diseases: Revised and Updated Consensus Statement of the Working Group on Management of Congenital Heart Diseases. Abridged Secondary Publication. Indian Pediatr. el 15 de febrero de 2020;57(2):143–57.
12. Eckerström F, Nyboe C, Redington A, Hjortdal VE. Lifetime Burden of Morbidity in Patients With Isolated Congenital Ventricular Septal Defect. J Am Heart Assoc. el 3 de enero de 2023;12(1):e027477.
13. Halloran KH, Talner NS, Browne MJ. A study of ventricular septal defect associated with aortic insufficiency. Am Heart J. marzo de 1965;69:320–6.
14. Nadas AS, Thilenius OG, Lafarge CG, Hauck AJ. Ventricular septal defect with aortic regurgitation: medical and pathologic aspects. Circulation. junio de 1964;29:862–73.
15. Layangool T, Kirawittaya T, Sangtawesin C. Aortic valve prolapse in subpulmonic ventricular septal defect. J Med Assoc Thail Chotmaihet Thangphaet. agosto de 2003;86 Suppl 3:S549-555.
16. Saleeb SF, Solowiejczyk DE, Glickstein JS, Korsin R, Gersony WM, Hsu DT. Frequency of development of aortic cuspal prolapse and aortic regurgitation in patients with subaortic ventricular septal defect diagnosed at <1 year of age. Am J Cardiol. el 1 de junio de 2007;99(11):1588–92.
17. Gasul BM, Dillon RF, Vrla V, Hait G. Ventricular septal defects; their natural transformation into the cyanotic or noncyanotic type of tetralogy of Fallot. J Am Med Assoc. el 22 de junio de 1957;164(8):847–53.
18. Soto B, Becker AE, Moulaert AJ, Lie JT, Anderson RH. Classification of ventricular septal defects. Br Heart J. marzo de 1980;43(3):332–43.
19. Themes UFO. Surgical Approaches for Common Congenital Heart Diseases [Internet]. Thoracic Key. 2022 [citado el 2 de noviembre de 2024]. Disponible en: https://thoracickey.com/surgical-approaches-for-common-congenital-heart-diseases/
20. Li D, Zhou X, Li M, An Q. Comparisons of perventricular device closure, conventional surgical repair, and transcatheter device closure in patients with perimembranous ventricular septal defects: a network meta-analysis. BMC Surg. el 26 de mayo de 2020;20(1):115.
21. Singab H, Elshahat MK, Taha AS, Ali YA, El-Emam AM, Gamal MA. Transcatheter versus surgical closure of ventricular septal defect: a comparative study. Cardiothorac Surg. el 20 de abril de 2023;31(1):8.
22. Xiao Y, Fan Z, Fang H, Tan W, Lu J, Jiang H. Comparison of efficacy and cost between transcatheter and surgical closure of secundum perimembranous ventricular septal defect. J Minim Invas Med. 2008;3:311–3.
23. Chen Y, Chen J, Niu T, Li Y, Ma M, Zhang Y. The therapeutic efficacy of interventional therapy and operation for ventricular septal defect. Ningxia Med J. 2010;32:1128–9.
24. Liu S, Chen F, Ding X, Zhao Z, Ke W, Yan Y, et al. Comparison of results and economic analysis of surgical and transcatheter closure of perimembranous ventricular septal defect. Eur J Cardio-Thorac Surg Off J Eur Assoc Cardio-Thorac Surg. diciembre de 2012;42(6):e157-162.
25. Tan CMJ, Lewandowski AJ. The Transitional Heart: From Early Embryonic and Fetal Development to Neonatal Life. Fetal Diagn Ther. 2020;47(5):373–86.
26. Mavroudis C, Backer CL, Anderson RH. Ventricular Septal Defect. En: Mavroudis C, Backer CL, editores. Pediatric Cardiac Surgery [Internet]. 1a ed. Wiley; 2023 [citado el 3 de noviembre de 2024]. p. 317–60. Disponible en: https://onlinelibrary.wiley.com/doi/10.1002/9781119282327.ch16
27. Hoffman JIE, Kaplan S. The incidence of congenital heart disease. J Am Coll Cardiol. el 19 de junio de 2002;39(12):1890–900.
28. Maître Azcárate MJ. [Ventricular septal defect with aortic regurgitation. An unsolved problem]. Rev Esp Cardiol. septiembre de 2002;55(9):897–9.
29. Fulton D, Saleeb S, Triedman J, Armbsby C. Isolated ventricular septal defects (VSDs) in infants and children: Management [Internet]. 2024. Disponible en: https://www.uptodate.com/contents/isolated-ventricular-septal-defects-vsds-in-infants-and-children-management?search=Isolated%20ventricular%20septal%20defects%20%28VSDs%29%20in%20infants%20and%20children%3A%20Management&source=search_result&selectedTitle=1%7E150&usage_type=default&display_rank=1
30. Instituto Nacional de Salud del Niño – San Borja. Guía de práctica clínica de manejo de la comunicación interventricular. Perú; 2016.
31. Kuo SM, Kang PL, Lyu JJ, Cheng KD, Hsieh KS. Repair of ventricular septal defect in infants without ventriculotomy. Australas J Card Thorac Surg. el 1 de agosto de 1992;1(2):27–30.
32. Talwar S, Keshri VK, Choudhary SK, Gupta SK, Ramakrishnan S, Juneja R, et al. Surgical strategies for patients with congenital heart disease and severe pulmonary hypertension in low/middle-income countries. Heart Asia. 2015;7(2):31–7.
33. Waqar T, Rizvi MFA, Nasir JA, Khan K. Surgical outcome of repair of aortic valve prolapse and regurgitation associated with ventricular septal defect. Pak J Med Sci. 2021;37(3):706–10.
34. Mukherji A, Ghosh S, Das D, Chattopadhyay A. Closure of ventricular septal defect in anatomically corrected malposition of great arteries: Case series with review of literature. Prog Pediatr Cardiol. el 1 de diciembre de 2020;59:101296.
35. Kleinman CS, Tabibian M, Starc TJ, Hsu DT, Gersony WM. Spontaneous regression of left ventricular dilation in children with restrictive ventricular septal defects. J Pediatr. junio de 2007;150(6):583–6.
36. Lévy M, Maurey C, Dinh-Xuan AT, Vouhé P, Israël-Biet D. Developmental expression of vasoactive and growth factors in human lung. Role in pulmonary vascular resistance adaptation at birth. Pediatr Res. mayo de 2005;57(5 Pt 2):21R-25R.
37. Mehta AV, Chidambaram B. Ventricular septal defect in the first year of life. Am J Cardiol. el 1 de agosto de 1992;70(3):364–6.
38. Pillai LS, Unnikrishnan D, Ahamed MZ. Study of clinical profile and outcome of ventricular septal defects diagnosed in infancy. Indian J Child Health. el 1 de octubre de 2019;06(09):485–9.
39. Deng X, Huang P, Luo J, Chen R, Yang G, Chen W, et al. Residual Shunts Following Isolated Surgical Ventricular Septal Defect Closure: Risk Factors and Spontaneous Closure. Pediatr Cardiol. el 1 de enero de 2020;41(1):38–45.
40. Penny DJ, Vick GW. Ventricular septal defect. Lancet Lond Engl. el 26 de marzo de 2011;377(9771):1103–12.
41. Seguro Social de Salud, EsSalud. Control del crecimiento y desarrollo del niño en el Seguro Social de Salud – EsSalud. Perú; 2024.
42. Chen D, Zhang Y, Liu J, Lin L, Shen F. Comparative study for clinical effect on ventricular septal defect in children between interventional treatment and surgical open thoracic operation. PJCCPVD. 2015;23:54–6.
43. Ece İ, Bağrul D, Kavurt AV, Terin H, Torun G, Koca S, et al. Transcatheter ventricular septal defect closure with LifetechTM Konar-MF occluder in infants under ten kilograms with only using venous access [Internet]. In Review; 2023 [citado el 11 de noviembre de 2024]. Disponible en: https://www.researchsquare.com/article/rs-3278632/v1
44. Saurav A, Kaushik M, Mahesh Alla V, White MD, Satpathy R, Lanspa T, et al. Comparison of percutaneous device closure versus surgical closure of peri-membranous ventricular septal defects: A systematic review and meta-analysis. Catheter Cardiovasc Interv Off J Soc Card Angiogr Interv. el 15 de noviembre de 2015;86(6):1048–56.
45. El-Kadeem S, El Nemr S, El Amrousy D, Zoair A. Comparison of transcatheter versus surgical closure of perimembranous ventricular septal defect in pediatric patients: A systematic review and meta-analysis. J Saudi Heart Assoc. octubre de 2019;31(4):188–97.
46. Yang J, Yang L, Yu S, Liu J, Zuo J, Chen W, et al. Transcatheter versus surgical closure of perimembranous ventricular septal defects in children: a randomized controlled trial. J Am Coll Cardiol. el 1 de abril de 2014;63(12):1159–68.
47. Shang XK, Zhong L, Lu R, Zhang GC, Liu M, Shen QS, et al. Comparison of Outcomes of Transcatheter and Surgical Procedure in Perimembranous Ventricular Septal Defect Patients with Tricuspid Regurgitation. Ann Acad Med Singapore. julio de 2016;45(7):322–5.
48. Laha S, Gangopadhyay D, Roy M, Singh A, Nandi D, Dutta J. Procedural outcomes of percutaneous closure of perimembranous and other ventricular septal defects using Konar-MF occluder and short-term follow-up. Ann Pediatr Cardiol [Internet]. abril de 2024 [citado el 8 de noviembre de 2024];17(2):101. Disponible en: https://journals.lww.com/aopc/fulltext/2024/17020/procedural_outcomes_of_percutaneous_closure_of.3.aspx
49. Incidence, Risk Factors, and Outcomes of Conduction Disturbances After Percutaneous Closure of Perimembranous Ventricular Septal Defects in Children and Adolescents: A Mid-term Follow-up | IJ Pediatrics | Full Text [Internet]. [citado el 8 de noviembre de 2024]. Disponible en: https://brieflands.com/articles/ijp-135528
50. Ece İ, Bağrul D, Kavurt AV, Terin H, Torun G, Koca S, et al. Transcatheter ventricular septal defect closure with LifetechTM Konar-MF occluder in infants under ten kilograms with only using venous access [Internet]. 2023 [citado el 8 de noviembre de 2024]. Disponible en: https://www.researchsquare.com/article/rs-3278632/v1
51. Stouffer GA, Uretsky BF. Hemodynamic changes of aortic regurgitation. Am J Med Sci. diciembre de 1997;314(6):411–4.
52. Edraki M, Nobakhti M, Naghshzan A, Amoozgar H, Amirghofran A, Ghasemzadeh B, et al. Mitral and aortic valve regurgitation following surgical and transcatheter perimembranous ventricular septal defect closure in children and adolescents: midterm outcomes. BMC Cardiovasc Disord [Internet]. el 15 de julio de 2022 [citado el 13 de noviembre de 2024];22(1):315. Disponible en: https://doi.org/10.1186/s12872-022-02757-9
53. Vázquez et al. – 2022 – Tratamiento de la Comunicación Interventricular (C.pdf [Internet]. [citado el 13 de noviembre de 2024]. Disponible en: https://www.iacs.es/wp-content/uploads/2022/04/02_2017_IACS_CIV-Informe.pdf
54. Saxena A, Relan J, Agarwal R, Awasthy N, Azad S, Chakrabarty M, et al. Indian guidelines for indications and timing of intervention for common congenital heart diseases: Revised and updated consensus statement of the Working group on management of congenital heart diseases. Ann Pediatr Cardiol [Internet]. 2019 [citado el 8 de noviembre de 2024];12(3):254. Disponible en: https://journals.lww.com/10.4103/apc.APC_32_19
55. Agasthi P, Graziano JN. Pulmonary Artery Banding. En: StatPearls [Internet] [Internet]. StatPearls Publishing; 2023 [citado el 13 de noviembre de 2024]. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK560838/
56. Hoseinikhah H, Moeinipour A, Zarifian A, Sobhan M, Andalibi S, Moeinipour Y, et al. Indications, Results and Mortality of Pulmonary Artery Banding Procedure: a Brief Review and Five- year Experiences. 2016;
57. Luna-López R, Ruiz Martín A, Escribano Subías P. Pulmonary arterial hypertension. Med Clin (Barc). el 24 de junio de 2022;158(12):622–9.
58. Hansmann G, Koestenberger M, Alastalo TP, Apitz C, Austin ED, Bonnet D, et al. 2019 updated consensus statement on the diagnosis and treatment of pediatric pulmonary hypertension: The European Pediatric Pulmonary Vascular Disease Network (EPPVDN), endorsed by AEPC, ESPR and ISHLT. J Heart Lung Transplant. el 1 de septiembre de 2019;38(9):879–901.
59. Lopes AA, Barst RJ, Haworth SG, Rabinovitch M, Dabbagh MA, Cerro MJ del, et al. Repair of congenital heart disease with associated pulmonary hypertension in children: what are the minimal investigative procedures? Consensus statement from the Congenital Heart Disease and Pediatric Task Forces, Pulmonary Vascular Research Institute (PVRI). Pulm Circ. junio de 2014;4(2):330.
60. Wood P. The Eisenmenger syndrome or pulmonary hypertension with reversed central shunt. I. Br Med J. el 20 de septiembre de 1958;2(5098):701–9.
61. Vongpatanasin W, Brickner ME, Hillis LD, Lange RA. The Eisenmenger syndrome in adults. Ann Intern Med. el 1 de mayo de 1998;128(9):745–55.
62. Frank BS, Ivy DD. Pediatric Pulmonary Arterial Hypertension. Pediatr Clin North Am. octubre de 2020;67(5):903–21.
63. Setianto BY, Hariawan H, Imawan R. Ventricular Septal Defect Closure with Perforated Patch in Large Ventricular Septal Defect with Severe Pulmonary Hypertension and Non Reactive Oxygen Test. ACI Acta Cardiol Indones [Internet]. el 9 de enero de 2017 [citado el 11 de noviembre de 2024];1(2). Disponible en: https://journal.ugm.ac.id/jaci/article/view/17813
64. Tooba R, Almoushref A, Tonelli AR. Is There Value in Repeating Inhaled Nitric Oxide Vasoreactivity Tests in Patients with Pulmonary Arterial Hypertension? Lung. febrero de 2020;198(1):87–94.
65. Evers PD, Quinn P, Critser PJ, Frank BS, Alnoor M, Armsby LB. Prognostic value of longitudinal vasoreactivity in pediatric pulmonary hypertension. Pulm Circ. el 1 de octubre de 2022;12(4):e12152.
66. Li Q, He Y, Zhang C, Gu H. Invasive Hemodynamic and Vasoreactivity Testing with Inhaled Iloprost in Children with Pulmonary Arterial Hypertension Associated with Congenital Heart Defects. Cardiol Discov. diciembre de 2023;3(4):232.
67. Shams KA, Ellahony DM, Halima AF, Elzayat RS. Effect of phosphodiesterase type 5 inhibitors on surgical outcome of ventricular septal defect and pulmonary hypertension patients. Egypt Heart J EHJ Off Bull Egypt Soc Cardiol. el 21 de mayo de 2024;76(1):60.
68. Zhang C, Li Q, Liu T, Gu H. Cardiac catheterization and pulmonary vasoreactivity testing in children with idiopathic pulmonary arterial hypertension. Chin J Pediatr. 2014;52(6):468–72.
69. Nawaytou H, Lakkaraju R, Stevens L, Reddy VM, Swami N, Keller RL, et al. Management of pulmonary vascular disease associated with congenital left-to-right shunts: A single-center experience. J Thorac Cardiovasc Surg. mayo de 2024;S0022522324004380.
Si tienes comentarios sobre el contenido de las guías de práctica clínica, puedes comunicarte con IETSI-EsSalud enviando un correo: gpcdireccion.ietsi@essalud.gob.pe

SUGERENCIAS
Si has encontrado un error en esta página web o tienes alguna sugerencia para su mejora, puedes comunicarte con EviSalud enviando un correo a evisalud@gmail.com


